ABSTRAK
Latar belakang
Risiko tinggi operasi reseksi untuk epilepsi hamartoma hipotalamus (HH) mendorong minat pada perawatan minimal invasif. Termokoagulasi frekuensi radio tiga dimensi yang dipandu stereo-elektroensefalografi (SEEG-3D RFTC) menawarkan pilihan alternatif. Kami menyelidiki kemanjuran, keamanan, dan faktor risiko prognostik teknologi ini.
Metode
Pasien dengan HH yang menjalani SEEG-3D RFTC dianalisis secara retrospektif. Implantasi elektroda stereo-array fokal kepadatan tinggi diadopsi. SEEG-3D RFTC dilakukan antara dua kontak yang berdekatan dari elektroda yang sama atau kontak yang berdekatan dari elektroda yang berbeda. Hasil dievaluasi secara terpisah untuk kejang klinis, kejang gelastik (GS), dan kejang non-gelastik (nGS). Analisis kelangsungan hidup Kaplan–Meier digunakan untuk menilai efektivitas pengobatan. Faktor risiko dianalisis menggunakan uji log-rank dan analisis regresi Cox.
Hasil
Enam puluh sembilan pasien didaftarkan. Rata-rata tindak lanjut adalah 41,00 ± 18,19 bulan. Kebebasan kejang diperoleh oleh 48/69 (69,57%) pasien untuk kejang klinis, 50/62 (80,65%) pasien untuk GS, dan 41/54 (75,93%) pasien untuk nGS. Prosedur pembedahan ditoleransi dengan baik. Dalam penelitian ini, proporsi pasien yang mengalami komplikasi jangka panjang adalah 10,14%. Persentase ablasi HH ( p = 0,003; rasio bahaya 0,956, interval kepercayaan 95% 0,928–0,985) dan ablasi perlekatan HH ( p = 0,001; rasio bahaya 0,931, interval kepercayaan 95% 0,892–0,970) secara signifikan terkait dengan hasil kejang.
Kesimpulan
SEEG-3D RFTC yang dioptimalkan merupakan pilihan yang efektif dan aman untuk epilepsi terkait HH dan sangat cocok untuk digunakan di tempat yang tidak tersedia terapi termal interstisial laser. Ablasi lengkap HH dan lokasi perlekatan sangat penting untuk hasil yang baik.
1 Pendahuluan
Hamartoma hipotalamus (HH) adalah lesi non-neoplastik kongenital langka dengan perkiraan insidensi 1/50.000–1/100.000. Kondisi ini biasanya muncul pada masa kanak-kanak, dengan epilepsi, pubertas prekoks, dan disfungsi kognitif sebagai gejala yang paling umum dan khas. Kejang yang terkait dengan HH sering kali ditandai dengan kejang gelastik (GS) dan sering kali disertai dengan jenis kejang lainnya (nGS), termasuk kejang fokal dan/atau umum [ 1 ]. Karena kejang yang disebabkan oleh HH cukup resistan terhadap obat, perawatan bedah dianggap penting untuk mengendalikan kejang yang terkait dengan HH. Namun, mencapai pemutusan hubungan HH yang efektif dan aman dari hipotalamus normal tetap menjadi tantangan yang signifikan [ 2 , 3 ].
Operasi terbuka secara tradisional merupakan pendekatan utama untuk pengobatan HH; namun, meskipun terdapat berbagai pendekatan pembedahan, tingkat komplikasi tetap tinggi, melebihi 30% [ 4 – 6 ]. Sebaliknya, teknik invasif minimal seperti terapi termal interstisial laser (LITT), termokoagulasi, dan radiosurgery Gamma Knife menawarkan tingkat invasif yang lebih rendah dan semakin menjadi pengobatan lini pertama untuk HH.
Penelitian sebelumnya telah menguji efikasi teknik-teknik ini. Gamma Knife Surgery (GKS) telah menunjukkan hasil jangka panjang dalam pengendalian epilepsi dengan profil keamanan yang baik; namun, hanya 39,6% pasien yang mencapai hasil Engel I [ 7 ]. LITT telah menunjukkan hasil yang baik dalam pengendalian kejang, sedangkan studi kohort jangka panjang skala besar belum dipublikasikan [ 8 , 9 ]. Stereo-electroencephalography-guided radiofrequency thermocoagulation (SEEG-RFTC) juga merupakan pendekatan minimal invasif dan telah diterapkan secara luas dalam operasi epilepsi. Tim kami melaporkan bukti primer pertama yang mendukung efikasi SEEG-RFTC pada HH [ 10 ]. Namun, secara luas diakui bahwa volume ablasi terbatas dari protokol RFTC konvensional membatasi efikasinya dalam pengendalian kejang [ 11 ]. kami mengoptimalkan implantasi SEEG dan prosedur RFTC dengan menggunakan elektroda cross-SEEG dengan protokol RFTC tiga dimensi (3D) [ 12 ]. Percobaan in vitro kami sebelumnya menunjukkan bahwa RFTC 3D dapat mencapai 1,81–2,12 kali volume ablasi dibandingkan dengan protokol konvensional. SEEG-3D RFTC yang dioptimalkan ini telah berhasil digunakan dalam berbagai jenis epilepsi, menghasilkan hasil kejang yang baik [ 13 , 14 ]. Dalam penelitian ini, kami menganalisis secara retrospektif pasien dengan HH yang diobati menggunakan protokol optimal yang sama.
Sepengetahuan kami, ini merupakan kelompok pasien terbesar dengan epilepsi terkait HH yang diobati menggunakan SEEG-3D RFTC yang dioptimalkan. Kami menganalisis hasil kejang jangka panjang, melakukan evaluasi terpisah terhadap remisi kejang pada GS dan nGS, dan mengidentifikasi faktor risiko yang terkait dengan prognosis bedah. Studi ini bertujuan untuk memberikan pilihan pengobatan minimal invasif yang efektif dan layak secara teknis bagi pasien dengan epilepsi terkait HH.
2 Metode
2.1 Pasien
Studi retrospektif ini mencakup semua pasien dengan epilepsi HH yang dirawat oleh SEEG-3D RFTC antara Juli 2015 dan Juni 2021 di Rumah Sakit Xuanwu, Capital Medical University, Beijing, Tiongkok. Persetujuan tertulis diperoleh dari pasien untuk publikasi laporan kasus ini dan gambar yang menyertainya. Faktor klinis meliputi jenis kelamin, usia, durasi epilepsi, pubertas prekoks (PP), klasifikasi HH, volume HH, ukuran HH (diameter maksimum dalam dimensi apa pun), dan operasi sebelumnya. Faktor bedah meliputi volume ablasi, persentase ablasi HH, dan persentase ablasi perlekatan HH. Kasus akan dikecualikan jika memenuhi salah satu kriteria berikut: (1) catatan medis epilepsi tidak memiliki informasi yang dikonfirmasi tentang perkembangan penyakit; (2) ada riwayat perawatan bedah saraf atau radiosurgical sebelumnya; (3) data pencitraan resonansi magnetik (MRI) resolusi tinggi yang diperlukan untuk analisis anatomi tidak tersedia; (4) Analisis MRI mengungkapkan adanya kelainan otak lainnya pada pasien. Studi ini disetujui oleh Komite Etika Rumah Sakit Xuanwu dan dilakukan sesuai dengan standar etika, termasuk Deklarasi Helsinki.
2.2 Pemeriksaan Prabedah
Semua menjalani penilaian menyeluruh yang terdiri dari pemantauan video-elektroensefalogram (EEG) dan berbagai pemeriksaan neuroimaging, termasuk MRI kepala 3.0-T dan pemindaian tomografi emisi positron. Berdasarkan pemindaian MRI koronal, HH dikategorikan sebagai intrahipotalamus, parahipotalamus, campuran dengan perlekatan unilateral, atau campuran dengan perlekatan bilateral [ 15 ]. Hasil pemeriksaan dipresentasikan kepada tim multidisiplin untuk diskusi lebih lanjut. Strategi untuk penerapan elektroda SEEG dirancang setelah diagnosis epilepsi terkait HH dan keputusan untuk menjalani operasi SEEG-3D RFTC. Alur kerja penelitian ini ditunjukkan pada Gambar 1 .
GAMBAR 1
Buka di penampil gambar
Presentasi PowerPoint
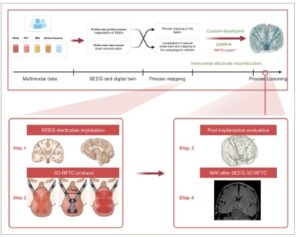
Alur kerja dari SEEG-3D RFTC yang dioptimalkan. ATAS: Alur kerja umum dari SEEG-3D RFTC yang dioptimalkan. MDT, tim multidisiplin; SOZ, zona onset kejang. Bawah: SEEG-3D RFTC yang dioptimalkan untuk epilepsi HH. Ilustrasi skema protokol implantasi elektroda SEEG stereo-crossed di HH. Elektroda SEEG ditanamkan ke HH melalui pendekatan paraventrikular. Langkah 1: Pandangan koronal dan sagital dari protokol implantasi elektroda. Langkah 2: Protokol RFTC 3D. Koagulasi bipolar pada masing-masing dari dua kontak yang berdekatan di setiap elektroda dan koagulasi bipolar 3D dari kontak di elektroda SEEG crossover dengan jarak < 7 mm. Langkah 3: Evaluasi pasca-implantasi elektroda SEEG yang menargetkan HH melalui rekonstruksi MRI. Langkah 4: MRI setelah SEEG-3D RFTC. SEEG-3D RFTC, termokoagulasi frekuensi radio tiga dimensi yang dipandu stereo-elektroensefalografi; HH, hamartoma hipotalamus; MRI, pencitraan resonansi magnetik. Dibuat di BioRender.com .
2.3 Implantasi Elektroda SEEG dan Pemantauan EEG Intrakranial
Implantasi elektroda individual dirancang untuk orang yang menjalani SEEG-3D RFTC. MRI lapisan tipis yang disempurnakan (ketebalan irisan, 1 mm) dan CT lapisan tipis (ketebalan irisan, 1 mm) dilakukan sebelum perencanaan lintasan. Gambar diimpor ke sistem Robotized Stereotactic Assistant (ROSA, Medtech, Montpellier, Prancis) untuk menghasilkan fusi multimoda yang memvisualisasikan struktur vaskular dan kritis, membantu menghindari cedera vaskular.
Dengan anestesi umum, kepala pasien difiksasi dalam rangka stereotaktik. Lengan robotik sistem ROSA memandu pemegang elektroda ke setiap lintasan yang telah direncanakan sebelumnya, dan dokter bedah memasukkan elektroda secara berurutan melalui lubang burr. Elektroda (Alcis, Besancon, Prancis) dipasang menggunakan sistem ROSA. Setiap elektroda SEEG terdiri dari 5–15 kontak silinder yang terbuat dari paduan platinum-iridium, dengan setiap kontak berukuran panjang 2 mm dan diameter 0,8 mm. Jarak pusat ke pusat antara kontak adalah 3,5 mm.
Lintasan dirancang secara individual untuk mengoptimalkan pengambilan sampel dari HH dan perlekatan anatomisnya. Pendekatan paraventrikular lebih disukai untuk mencapai akses yang lebih luas ke lesi dan antarmukanya dengan ventrikel ketiga. Batas lesi ditentukan berdasarkan perbedaan intensitas sinyal antara HH dan dinding ventrikel pada MRI lapisan tipis. Setiap lintasan melewati girus frontal superior atau tengah dan berakhir di tepi medial HH.
Beberapa elektroda ditanamkan secara bilateral, dengan fokus pada penutupan struktur internal hamartoma. Strategi penanaman adalah memastikan bahwa jarak antara target elektroda kurang dari 7 mm, sehingga bidang ablasi yang tumpang tindih dapat terbentuk di antara kontak elektroda yang berdekatan. Desain ini memungkinkan pengambilan sampel dengan kepadatan tinggi dan lesi termal yang efektif. CT pascaoperasi dilakukan dalam waktu 24 jam untuk memverifikasi posisi elektroda. Pemantauan SEEG dimulai setelah mengonfirmasi keakuratan dan menyingkirkan komplikasi seperti pendarahan.
2.4 Akurasi Aplikasi
Lokasi kontak yang tepat dari elektroda yang ditanamkan diverifikasi menggunakan CT 3D pascaoperasi yang didaftarkan bersama dengan MRI 3D T1-weighted praoperasi. Data pencitraan lintasan perencanaan praoperasi dalam sistem robot diintegrasikan dengan CT pascaoperasi. Titik masuk ditetapkan sebagai posisi tengah tempat lintasan elektroda memasuki korteks, dan target ditetapkan sebagai posisi akhir ujung elektroda. Lintasan yang direncanakan dan aktual ditentukan dari bidang koronal, sagital, dan transversal. Jarak Euclidean tak bertanda antara titik masuk yang direncanakan dan aktual (kesalahan lokalisasi titik masuk [EPLE]) dan antara titik target yang direncanakan dan aktual (kesalahan lokalisasi titik target [TPLE]) diukur menggunakan fungsi pengukuran jarak dalam sistem perangkat lunak robot.
2.5 Pipa Hitung RFTC
Untuk meningkatkan presisi rekonstruksi elektroda, kami telah mengembangkan alur kerja RFTC Count. RFTC Count adalah alur kerja yang dirancang untuk memproses dan menganalisis data kontak elektroda untuk menyaring pasangan kontak kandidat yang memenuhi kriteria jarak tertentu, yang bertujuan untuk memberikan referensi untuk penanganan RFTC. Langkah-langkah spesifiknya adalah sebagai berikut: (1) Menghitung koordinat titik masuk dan titik target. Berdasarkan ukuran voksel yang dimasukkan oleh pengguna dan jumlah kontak elektroda pada setiap elektroda, hitung koordinat tiga dimensi titik masuk dan titik target untuk setiap elektroda. (2) Menentukan koordinat yang tepat dari setiap kontak. Untuk setiap elektroda, gunakan koordinat titik masuk dan titik target untuk membagi elektroda secara merata menurut jumlah kontak. Hal ini memungkinkan perhitungan yang akurat dari koordinat yang tepat dari setiap kontak.
2.6 Evaluasi Lesi Bedah dan Ablasi RFTC 3D
Pemilihan kontak elektroda ablasi didasarkan pada penilaian praoperasi dan pemantauan EEG intrakranial. Kriteria inklusi adalah (1) lokasi inisiasi epileptogenik selama onset kejang atau pelepasan epilepsi signifikan selama periode interiktal dalam HH, dan (2) penilaian praoperasi kontak yang dirancang untuk ditempatkan di lokasi pemasangan HH. Kontak yang terletak < 2 mm dari pembuluh darah dikecualikan.
Operasi dilakukan dalam keadaan sadar, dan kontak terkait dihubungkan ke sistem pembangkit RFTC R200BM1 (Beijing Neo Science Co., Beijing, Tiongkok). Ablasi dilakukan sebagai ablasi bipolar terlebih dahulu dengan pulsa pra-ablasi 2 W selama 40 detik, diikuti oleh dua pulsa 3 W selama 60 detik antara dua kontak yang berdekatan pada elektroda yang sama. Kemudian, ablasi 3D dilakukan pada kontak dengan jarak < 7 mm pada elektroda paralel dan silang selama dua pulsa 3 W selama 60 detik. EEG intrakranial direkam selama 10 menit setelah ablasi. Sekrup pemandu dan elektroda diekstraksi setelah memastikan tidak ada kelainan atau pelepasan muatan intrakranial.
Volume lesi RFTC 3D dievaluasi menggunakan data MRI pascaoperasi yang diproses dalam perangkat lunak 3D Slicer (versi 4.10.2). Lesi ablasi disegmentasi secara manual irisan demi irisan untuk menggambarkan batas-batasnya; rekonstruksi kemudian dibuat, dan volume lesi dihitung secara otomatis. Persentase ablasi HH dihitung dengan membandingkan volume lesi RFTC 3D dengan volume HH yang diukur sebelum operasi, yang disegmentasi dan direkonstruksi menggunakan metode yang sama. Persentase ablasi perlekatan HH dinilai pada irisan MRI yang menunjukkan antarmuka maksimal antara HH dan hipotalamus (Gambar 2 ).

GAMBAR 2
Buka di penampil gambar
Presentasi PowerPoint
Pengukuran praoperasi HH dan pengukuran pascaoperasi lesi RFTC 3D. (A) Pandangan aksial praoperasi HH. Pembesaran parsial menguraikan rentang HH. (B) Pandangan koronal praoperasi HH. Pembesaran parsial menunjukkan diameter maksimum HH. (C) Pandangan aksial pascaoperasi HH. Pembesaran parsial menguraikan rentang ablasi dan HH residual. V1 = Volume HH yang diukur, V2 = Volume lesi RFTC 3D yang diukur di HH. (D) Pandangan koronal pascaoperasi HH. Pembesaran parsial menunjukkan perlekatan HH dan rentang perlekatan RFTC 3D. L1 = Perlekatan maksimal antara HH dan hipotalamus, L2 = Rentang RFTC 3D pada perlekatan HH. HH, hamartoma hipotalamus; SEEG-3D RFTC, termokoagulasi frekuensi radio tiga dimensi yang dipandu elektroensefalografi stereo.
2.7 Tindak Lanjut dan Penilaian Hasil Kejang
Hasil dalam hal penekanan kejang dan komplikasi terkait pembedahan dievaluasi pada interval 6 bulan setelah prosedur. Hasil kejang dievaluasi secara terpisah untuk kejang klinis, GS, dan nGS, menurut klasifikasi hasil League Against Epilepsy (ILAE) [ 16 ]. ILAE I dianggap bebas kejang.
2.8 Analisis Statistik
Analisis statistik dilakukan menggunakan SPSS 26 (IBM, Armonk, NY). Durasi hingga terjadinya kejang pascaoperasi pertama ditetapkan sebagai titik akhir untuk analisis kelangsungan hidup Kaplan–Meier. Selain itu, kelangsungan hidup bebas kejang dianalisis untuk setiap faktor yang diselidiki. Variabel kategoris dibandingkan menggunakan uji log-rank. Variabel kontinu, termasuk usia saat operasi, usia saat kejang/GS/onset nGS, dan durasi epilepsi, dikotomi sepanjang median [ 17 ]. Ukuran HH dikotomi menggunakan diameter maksimum 15 mm [ 18 ]. Persentase ablasi HH dan ablasi perlekatan HH menjalani analisis Cox univariat sebagai variabel kontinu. Variabel dengan p < 0,2 dalam analisis univariat dimasukkan dalam analisis regresi Cox multivariat. Signifikansi statistik ditetapkan pada p < 0,05.
3 Hasil
3.1 Karakteristik Pasien
Enam puluh sembilan pasien (44 laki-laki dan 25 perempuan) yang menjalani SEEG-3D RFTC diikutsertakan, di antaranya 62 orang menderita GS dan 54 orang menderita nGS. Usia saat operasi dan onset kejang, serta durasi epilepsi masing-masing adalah 10,58 ± 8,85, 3,37 ± 3,83, dan 7,24 ± 7,17 tahun. Untuk pasien GS, usia saat operasi dan onset GS, serta durasi GS masing-masing adalah 9,84 ± 8,12, 2,94 ± 3,18, dan 6,79 ± 7,02 tahun. Bagi pasien nGS, usia saat operasi dan timbulnya nGS, serta durasi nGS masing-masing adalah 11,74 ± 9,36, 7,07 ± 5,80, dan 4,10 ± 5,22 tahun (Tabel 1 ).
TABEL 1. Profil pasien SEEG-3D RFTC dan hasil kejang.
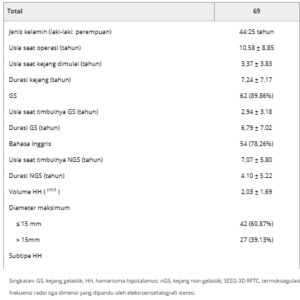
Diameter maksimum HH adalah < 15 mm pada 42 pasien dan > 15 mm pada 27 pasien. Volume rata-rata HH adalah 2,03 ± 1,69 cm [ 3 ]. Tipe campuran dengan perlekatan bilateral adalah subtipe yang paling banyak diamati, yaitu sebesar 33,33% (23/69), diikuti oleh tipe intrahipotalamus (23,19%, 16/69), tipe campuran dengan perlekatan unilateral (21,74%, 15/69), dan tipe parahipotalamus (21,74%, 15/69).
3.2 Implantasi SEEG dan Karakteristik RFTC 3D
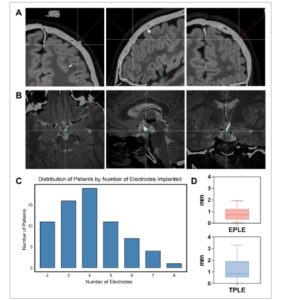
Dalam penelitian ini, semua implantasi elektroda menargetkan daerah HH. Sebanyak 279 elektroda ditanamkan, dengan 2–8 elektroda per implantasi. Kesalahan titik masuk dan titik target semua elektroda dianalisis secara statistik. TPLE adalah 1,15 ± 0,82 mm dan EPLE adalah 0,81 ± 0,51 mm. Distribusi jumlah elektroda yang ditanamkan dan kesalahan akurasi SEEG ditunjukkan pada Gambar 3 .
GAMBAR 3
Buka di penampil gambar
Presentasi PowerPoint
Karakteristik implantasi elektroda SEEG. (A) Penentuan EPLE. Pandangan aksial, sagital, dan koronal dari lintasan elektroda yang direncanakan dan aktual di titik masuk. (B) Penentuan TPLE. Pandangan aksial, sagital, dan koronal dari lintasan elektroda yang direncanakan dan aktual di titik target. (C) Distribusi pasien berdasarkan jumlah elektroda SEEG yang ditanamkan. (D) EPLE dan TPLE elektroda SEEG dalam penelitian ini. EPLE = 0,81 ± 0,51 mm dan TPLE = 1,15 ± 0,82 mm. SEEG, stereo-elektroensefalografi; EPLE, kesalahan lokalisasi titik masuk; TPLE, kesalahan lokalisasi titik target.
Lesi RFTC 3D direkonstruksi dan volumenya diukur. Volume RFTC 3D rata-rata adalah 1,39 ± 1,10 cm3 [ 3 ]. Berdasarkan volume HH yang diukur sebelum operasi, persentase rata-rata ablasi HH adalah 72,98% ± 16,49%. Luas ablasi pada lokasi perlekatan HH mencerminkan derajat pemutusan HH; persentase rata-rata ablasi perlekatan HH adalah 63,41% ± 12,01% (Tabel 2 ). Kasus-kasus khas RFTC 3D ditunjukkan pada Gambar 4 .
TABEL 2. Hasil pasien SEEG-3D RFTC.
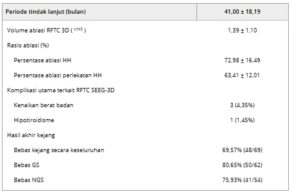
Singkatan: GS, kejang gelastik; HH, hamartoma hipotalamus; nGS, kejang non-gelastik; SEEG-3D RFTC, termokoagulasi frekuensi radio tiga dimensi yang dipandu oleh elektroensefalografi stereo.
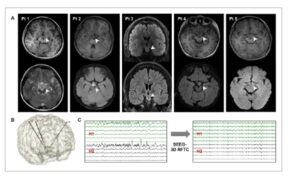
GAMBAR 4
Buka di penampil gambar
Presentasi PowerPoint
Kasus-kasus khas SEEG-3D RFTC pada HH. (A) MRI pra- dan pasca-operasi dari lima pasien representatif yang menggambarkan area lesi yang dibuat oleh SEEG-3D RFTC. (B) Rekonstruksi elektroda SEEG pada Pt 1. (C) Pemantauan SEEG sebelum dan sesudah 3D RFTC mengungkapkan hilangnya aktivitas epileptiform secara menyeluruh di dalam HH. SEEG-3D RFTC, termokoagulasi frekuensi radio tiga dimensi yang dipandu oleh stereo-elektroensefalografi; HH, hamartoma hipotalamus; Pt, pasien.
3.3 Hasil Kejang
Tindak lanjut rata-rata adalah 41,00 ± 18,19 bulan (12–85 bulan). Untuk semua pasien, 69,57% (48/69) bebas kejang pada akhir tindak lanjut, dengan waktu bertahan hidup bebas kejang rata-rata 59,45 ± 4,69 bulan (interval kepercayaan [CI] 95%, 50,26–68,64 bulan). Sebagian besar kejadian kejang berulang (80,95%) terjadi dalam waktu 6 bulan setelah operasi. Tingkat bebas kejang adalah 89,86%, 78,26%, dan 75,36% pada 1, 3, dan 6 bulan, masing-masing, dan tetap stabil selama tindak lanjut (Gambar 5 ).
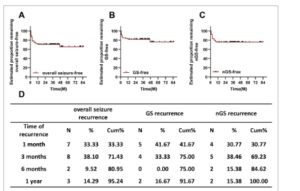
GAMBAR 5
Buka di penampil gambar
Presentasi PowerPoint
Analisis kurva kelangsungan hidup Kaplan–Meier setelah SEEG-3D RFTC. (A) Kurva kelangsungan hidup bebas kejang secara keseluruhan, (B) bebas GS, dan (C) bebas nGS setelah SEEG-3D RFTC. (D) Tabel mencantumkan jumlah dan rasio kekambuhan pada setiap titik waktu. GS, kejang gelastik; nGS, kejang non-gelastik; SEEG-3D RFTC, termokoagulasi frekuensi radio tiga dimensi yang dipandu oleh stereo-elektroensefalografi; Kum, kumulatif.
Bagi 62 pasien GS, waktu bertahan hidup rata-rata bebas GS adalah 68,12 ± 4,43 bulan (IK 95%, 59,43–76,80 bulan). Dari pasien-pasien ini, 91,94%, 85,48%, dan 85,48% bebas GS pada bulan ke-1, ke-3, dan ke-6, secara berurutan. Hasil GS tetap baik, dan 80,65% (50/62) bebas GS pada akhir tindak lanjut (Gambar 5 ).
Untuk 54 pasien nGS, waktu bertahan hidup rata-rata bebas nGS adalah 64,67 ± 4,68 bulan (95% CI, 55,50–73,83 bulan). Dari pasien-pasien ini, 92,59%, 83,33%, dan 79,63% bebas nGS pada 1, 3, dan 6 bulan, berturut-turut. Hasil nGS juga tetap stabil dalam jangka panjang, dengan 75,93% (41/54) bebas nGS pada akhir tindak lanjut (Gambar 5 ). Prosedur dan hasil pasien ditunjukkan di bawah ini (Gambar 6 ).

GAMBAR 6
Buka di penampil gambar
Presentasi PowerPoint
Hasil GS dan nGS setelah SEEG-3D RFTC. Diagram alir yang menunjukkan operasi berulang dan hasil SEEG-3D RFTC sehubungan dengan GS dan nGS pada 69 pasien. Kebebasan GS dan kebebasan nGS secara keseluruhan dicapai pada masing-masing 50 (80,65%) dan 41 (75,93%) pasien. GS, kejang gelastik; nGS, kejang non-gelastik; SEEG-3D RFTC, termokoagulasi frekuensi radio tiga dimensi yang dipandu oleh stereo-elektroensefalografi.
3.4 Keamanan Bedah
Komplikasi dirangkum dalam Tabel 2. Semua pasien mentoleransi prosedur dengan baik, tanpa komplikasi yang diamati terkait dengan implantasi SEEG.
Setelah SEEG-3D RFTC, semua pasien menjalani pemindaian CT dalam waktu 24 jam, yang menunjukkan perubahan kepadatan rendah di daerah ablasi. Meskipun terjadi berbagai tingkat edema di lokasi pemasangan HH, tidak ada gejala signifikan yang diamati, dan edema berangsur-angsur membaik.
Komplikasi yang terkait dengan RFTC 3D sebagian besar bersifat jangka pendek, tujuh pasien (10,14%) mengalami hipertermia sementara (> 38°C). Dua pasien (2,90%) mengalami gangguan memori jangka pendek. Empat pasien (5,80%) mengalami diabetes insipidus. Pasien-pasien ini mencapai remisi lengkap setelah perawatan konservatif. Oleh karena itu, komplikasi tersebut dianggap sebagai komplikasi ringan.
Komplikasi yang memerlukan penanganan jangka panjang diklasifikasikan sebagai komplikasi mayor. Empat pasien (5,80%) mengalami komplikasi mayor (peningkatan berat badan [ n = 3] dan hipotiroidisme [ n = 1]) (Tabel 2 ).
3.5 Faktor Risiko Terkait dengan Hasil Kejang
Untuk keseluruhan pasien dengan epilepsi HH, analisis univariat menunjukkan bahwa operasi sebelumnya, persentase ablasi HH, dan persentase ablasi perlekatan HH berhubungan secara signifikan dengan terbebasnya kejang setelah SEEG-3D RFTC (Tabel S1 ). Model regresi Cox multivariat mengungkapkan bahwa persentase ablasi HH dan ablasi perlekatan HH merupakan faktor risiko yang signifikan (Tabel 3 ).
TABEL 3. Faktor risiko epilepsi HH yang diobati dengan SEEG-3D RFTC.
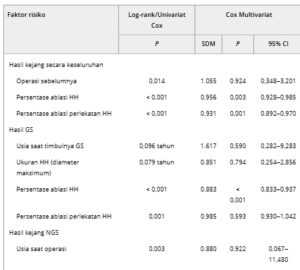
Singkatan: CI, interval kepercayaan; GS, kejang gelastik; HH, hamartoma hipotalamus; HR, rasio bahaya; nGS, kejang non-gelastik; RCS, spline kubik terbatas; SEEG-3D RFTC, termokoagulasi frekuensi radio tiga dimensi yang dipandu elektroensefalografi stereo.
Untuk hasil GS, persentase ablasi HH dan persentase ablasi perlekatan HH berhubungan signifikan dengan bebas dari GS menurut analisis univariat (Tabel S2 ). Akan tetapi, model regresi Cox multivariat menunjukkan bahwa satu-satunya faktor risiko signifikan untuk bebas dari GS adalah persentase ablasi HH (Tabel 3 ).
Untuk hasil NGS, usia saat operasi dan timbulnya NGS, durasi NGS, operasi sebelumnya, dan persentase ablasi HH dan ablasi perlekatan HH secara signifikan dikaitkan dengan terbebasnya NGS menurut analisis univariat (Tabel S3 ). Analisis regresi Cox multivariat menunjukkan bahwa persentase ablasi perlekatan HH merupakan satu-satunya faktor signifikan yang dikaitkan dengan terbebasnya NGS (Tabel 3 ).
4 Diskusi
Dalam penelitian ini, kami menggunakan teknologi SEEG-3D RFTC yang dioptimalkan dalam menangani HH dan melaporkan hasil tindak lanjut jangka panjang. Hasil kejang dievaluasi secara terpisah untuk kejang secara keseluruhan, GS, dan nGS. Sebagian besar kekambuhan kejang setelah SEEG-3D RFTC muncul dalam waktu 1 tahun. Analisis prognosis mengungkapkan bahwa persentase ablasi HH dan ablasi perlekatan HH merupakan faktor risiko yang secara signifikan memengaruhi pengendalian kejang secara keseluruhan.
4.1 Efektivitas SEEG-3D RFTC pada Epilepsi HH
SEEG yang disilangkan secara stereo memungkinkan cakupan kepadatan tinggi pada HH dan lokasi perlekatannya. Pengaturan ini memungkinkan penyelidikan jalur listrik rumit antara HH dan jaringan epilepsi interkortikal. Ini juga berfungsi sebagai dasar untuk protokol RFTC 3D.
Protokol SEEG-3D RFTC yang dioptimalkan bertujuan untuk memutus lesi HH melalui ablasi in situ di dalam HH itu sendiri dan tempat perlekatan [ 19 ]. Keuntungan dari protokol 3D RFTC yang dimodifikasi ini telah diverifikasi oleh tim peneliti kami melalui serangkaian eksperimen ex vivo dan in vivo yang komprehensif. Investigasi ini memberikan bukti bahwa teknologi 3D RFTC dapat mencapai jarak ablasi maksimum 7 mm [ 12 ]. Dalam aplikasi klinis, teknik yang dioptimalkan ini telah divalidasi pada sklerosis hipokampus, epilepsi insula, dan bentuk epilepsi fokal lainnya. Ini telah menunjukkan pemberantasan total fokus epileptogenik dan mencapai hasil pengendalian kejang yang memuaskan [ 13 , 14 ]. Dalam kasus HH, sebagian besar kasus epilepsi muncul dari tumor itu sendiri, dan fokus epilepsi terdefinisi dengan baik dan terbatas [ 20 ]. Sementara itu, melalui pemanfaatan elektroda SEEG yang dirancang silang dan 3D RFTC, adalah mungkin untuk mencapai ablasi total sebagian besar HH. Oleh karena itu, kami percaya bahwa pasien dengan epilepsi HH sangat cocok untuk SEEG-3D RFTC.
Studi ini lebih jauh memperkuat perspektif kami. Tingkat bebas kejang secara keseluruhan mencapai 69,57% di antara 69 pasien selama tindak lanjut rata-rata 41,00 bulan, yang menunjukkan efek terapi yang memuaskan dan stabil dari SEEG-3D RFTC dalam mengobati HH. Dibandingkan dengan studi LITT sebelumnya, 80% pasien dengan GS dan 56% pasien dengan nGS mencapai kebebasan kejang [ 21 ]; protokol SEEG-3D RFTC yang dioptimalkan menunjukkan efektivitas yang sebanding dalam hal kontrol kejang, dengan tingkat bebas GS dan nGS masing-masing sebesar 80,65% dan 75,93%. Dibandingkan dengan penelitian sebelumnya pada SEEG-RFTC, studi kami juga menunjukkan keuntungan yang berbeda. Liu et al. mencoba untuk meningkatkan prognosis SEEG-RFTC dengan berfokus pada ablasi perlekatan HH dan mencapai 70,4% Engel I pada 27 pasien [ 22 ]. mengadopsi protokol ablasi silang yang serupa dan mencapai hasil bedah yang baik pada 28 pasien [ 18 ]. Penelitian sebelumnya memberikan bukti awal tentang kelayakan SEEG-RFTC pada HH, dan penelitian kami memverifikasi kemanjuran yang lebih unggul dari SEEG-3D RFTC yang dioptimalkan pada HH dengan kelompok pasien yang lebih besar dan tindak lanjut yang lebih lama.
SEEG-3D RFTC juga mengungguli perawatan bedah lain dalam pengendalian kejang, termasuk kraniotomi dan GKS. Studi kraniotomi sebelumnya menunjukkan bahwa reseksi lengkap HH tidak dapat dicapai pada 38,5%–65,4% pasien dan tingkat bebas kejang bervariasi dari 15% hingga 54% [ 23 – 25 ]. Meskipun GKS relatif aman dan dapat dioperasikan dalam beberapa tahap, efektivitas pengendalian kejang memerlukan peningkatan. Uji coba prospektif yang mengevaluasi keamanan dan kemanjuran GKS menunjukkan bahwa 39,6% pasien mencapai hasil kelas I Engel, sementara 58,3% memerlukan perawatan kedua [ 7 ]. Penggunaan rutin robot bedah secara signifikan meningkatkan presisi implantasi SEEG, akibatnya berkontribusi pada peningkatan kemanjuran dalam ablasi dan pengendalian kejang.
MRI-stereotactic radiofrequency thermocoagulation (SRT) adalah pilihan ablasi serupa lainnya untuk HH. Kameyama et al. menunjukkan bahwa tingkat bebas kejang, bebas GS, dan bebas nGS secara keseluruhan masing-masing adalah 71%, 86%, dan 78,9% [ 15 , 26 ] . Namun, baik LITT maupun SRT tidak dapat secara langsung mengonfirmasi asal epileptogenik pada HH. Secara klinis, kami mengamati bahwa beberapa pasien HH memiliki onset kejang non-HH, meningkatkan kekhawatiran tentang potensi pengobatan berlebihan. Sebaliknya, SEEG-3D RFTC memungkinkan konfirmasi elektrofisiologi intraoperatif dan ablasi yang ditargetkan [ 26 , 27 ]. Kemampuannya untuk memetakan aktivitas epileptogenik waktu nyata menawarkan keuntungan utama dibandingkan pendekatan berbasis anatomi murni. Shirozu et al. menunjukkan bahwa batas elektrofisiologis antara HH dan hipotalamus sangat sesuai dengan batas yang ditentukan MRI, dan bahwa zona epileptogenik paling aktif berada di dekat antarmuka ini [ 28 ]. Lebih lanjut, Scholly et al. melaporkan bahwa pada beberapa pasien HH, kejang dapat berasal dari atau berkembang ke area neokorteks independen melalui proses seperti pemicu epileptogenesis sekunder [ 29 ]. SEEG saat ini merupakan satu-satunya alat yang mampu mengidentifikasi secara langsung jaringan iktogenik yang tersebar luas tersebut. Dengan demikian, ablasi yang dipandu SEEG tidak hanya dapat meningkatkan akurasi penargetan tetapi juga mencegah pengobatan yang kurang atau berlebihan pada pasien dengan pola penyebaran kejang yang atipikal.
4.2 Keamanan SEEG-3D RFTC pada Epilepsi HH
Dalam studi ini, SEEG-3D RFTC terbukti aman dan praktis. Komplikasi yang terkait dengan prosedur ini sebagian besar bersifat jangka pendek, termasuk hipertermia sementara, gangguan memori jangka pendek, disfungsi hipofisis, dan penambahan berat badan. Komplikasi jangka panjang hanya diamati pada empat pasien. Konsisten dengan studi sebelumnya tentang RFTC dan SRT, hipertermia merupakan komplikasi yang paling umum. Namun, Wang et al. tidak mengamati hipertermia dalam studi mereka [ 18 ]. Studi kami sengaja mencakup ablasi perlekatan HH, dan 3D RFTC menghasilkan kerusakan yang lebih luas, yang dapat berkontribusi pada konduksi panas di hipotalamus dan mengakibatkan hipertermia pascaoperasi.
Dibandingkan dengan intervensi bedah lainnya, SEEG-RFTC menawarkan keuntungan unik, khususnya dalam presisi dan keamanan fungsional. Dalam kraniotomi untuk HH, sebagian besar pasien mengalami setidaknya hipertermia sementara, dan tingkat komplikasi bedah tetap di atas 30%, bahkan dengan navigasi intraoperatif [ 30 ]. Akibatnya, pendekatan invasif minimal seperti LITT dan SEEG-3D RFTC telah mendapatkan perhatian yang semakin meningkat. LITT, meskipun presisinya dipandu MRI, memerlukan pengiriman energi tinggi, yang meningkatkan risiko difusi termal [ 31 ]. Santiago et al. melaporkan bahwa LITT dapat menyebabkan kerusakan di luar batas yang dimaksudkan, yang menyebabkan komplikasi serius seperti hemiplegia [ 32 ]. Xu et al. menemukan tingkat disfungsi jangka pendek dan jangka panjang masing-masing sebesar 39% dan 29% [ 21 ]. Risiko tambahan termasuk gangguan memori, hipotiroidisme tertunda, dan obesitas hipotalamus, khususnya pada lesi yang lebih besar. Sebaliknya, SEEG-3D RFTC memungkinkan ablasi bertahap dan dapat disesuaikan yang dipandu oleh umpan balik elektrofisiologis waktu nyata. Ukuran dan lintasan lesi dapat dimodifikasi selama operasi, sehingga mengurangi risiko cedera yang tidak diinginkan. Dilakukan dalam keadaan sadar dan disesuaikan dengan pemetaan fungsional, SEEG-RFTC meningkatkan keamanan dan kemampuan beradaptasi dalam kasus-kasus yang secara anatomis kompleks.
4.3 Faktor Risiko yang Mempengaruhi Pengendalian Kejang SEEG-3D RFTC pada HH
Kami mengamati korelasi signifikan antara hasil SEEG-3D RFTC pada epilepsi HH dan tingkat pemutusan perlekatan HH dan penghancuran HH, yang menunjukkan bahwa pemutusan dan ablasi lengkap HH sangat penting untuk pengendalian kejang; bahkan sejumlah kecil jaringan residual dapat menyebabkan kekambuhan kejang, konsisten dengan temuan Kameyama et al. [ 15 ]. Lebih jauh lagi, 80% kekambuhan terjadi dalam 6 bulan pascaoperasi, menunjukkan bahwa efek terapi SEEG-3D RFTC stabil jika penghancurannya lengkap.
Epilepsi terkait HH muncul dengan jaringan epileptogenik yang sama sekali berbeda pada GS dan nGS [ 32 ]. Asal mula gejala nGS mungkin sekunder terhadap jaringan di luar HH, di mana pelepasan epileptiform dari HH menyebabkan GS dan menciptakan koneksi abnormal dengan hipotalamus. Akibatnya, jaringan epileptogenik baru terbentuk secara independen, yang mengarah ke nGS [ 33 ]. Oleh karena itu, hasil GS dan nGS dibahas secara terpisah dalam penelitian ini.
Perbedaan ini didukung oleh bukti pencitraan dan elektrofisiologi. Studi menggunakan [18F]-FDG PET dan rs-fMRI telah menunjukkan bahwa pasien nGS sering menunjukkan hipometabolisme atau konektivitas yang berubah di daerah ekstra-hipotalamus, termasuk korteks cingulate, lobus temporal anterior, dan operkulum frontal [ 34 , 35 ]. Rekaman SEEG mengungkapkan bahwa sementara GS biasanya berasal secara fokal dalam HH, nGS melibatkan onset kortikal yang luas atau independen, terutama di daerah frontal dan temporal medial. Selain itu, propagasi HH-ke-korteks yang sinkron atau berurutan lebih lanjut mendukung HH sebagai pendorong epileptogenesis sekunder [ 36 ]. Temuan ini menggarisbawahi bahwa nGS bukan hanya perpanjangan dari GS tetapi manifestasi berbeda dari evolusi jaringan terkait HH.
Persentase ablasi HH merupakan satu-satunya faktor risiko penting untuk GS. Studi ablasi laser oleh Boerwinkle et al. menegaskan bahwa, terlepas dari ukuran HH, kebebasan yang baik dari kejang konsisten jika ablasi laser mencapai penghancuran total [ 37 ]. Penelitian kami mencapai hasil serupa dengan pengaturan elektroda kepadatan tinggi secara lokal dan RFTC 3D.
Sebaliknya, persentase ablasi perlekatan HH lebih penting untuk nGS. Meskipun nGS sering menunjukkan jaringan epilepsi yang kompleks, penelitian sebelumnya telah mengonfirmasi bahwa HH merupakan nodus yang penting. Memutuskan perlekatan masih masuk akal untuk prognosis. Kameyama dkk. menyarankan bahwa memutuskan perlekatan dapat menghasilkan hasil yang baik pada pasien dengan HH besar [ 38 ].
Beberapa penelitian telah menunjukkan bahwa LITT cukup efisien dalam mengobati HH, dan tujuan kami bukanlah untuk mengganti penggunaan LITT dengan SEEG-3D RFTC. Akan tetapi, dibandingkan dengan LITT, pemasangan elektroda SEEG dan penggunaan 3D RFTC lebih mudah beradaptasi dan hemat biaya. Melalui SEEG-3D RFTC yang dimodifikasi ini, kami juga telah meningkatkan efek ablasi dan memperbaiki prognosis. Kami berharap bahwa SEEG-3D RFTC akan menawarkan pilihan alternatif bagi individu di daerah yang tidak mudah dijangkau oleh LITT, dan penelitian ini dapat menawarkan panduan praktis untuk penerapan SEEG-3D RFTC.
5 Keterbatasan
Studi ini merupakan analisis retrospektif yang dilakukan di satu pusat. Tidak ada kelompok kontrol yang cocok yang menerima perawatan alternatif (seperti LITT atau operasi terbuka) yang ditetapkan, yang membatasi kemungkinan untuk membandingkan secara langsung kemanjuran dan keamanan di antara berbagai teknik bedah. Oleh karena itu, studi prospektif multipusat di masa mendatang diperlukan untuk lebih memvalidasi generalisasi, efektivitas jangka panjang, dan batasan keamanan teknik ini.
6 Kesimpulan
SEEG-3D RFTC merupakan pengobatan minimal invasif yang efektif, aman, dan stabil untuk epilepsi terkait HH dan sangat cocok untuk promosi di daerah-daerah yang tidak menyediakan LITT. Ablasi HH dan lokasi perlekatan sangat penting untuk pengendalian kejang, dan meningkatkan rasio ablasi merupakan kunci untuk mencapai kebebasan kejang. Konsep penelitian ini juga berlaku untuk prosedur minimal invasif lainnya.

